Naatriumkarbonaaton valge lõhnatu pulber või osake normaaltemperatuuril. Sellel on veeimavus ja see neelab järk-järgult avatud õhust 1 mol/l vett (umbes =15 protsenti). Selle hüdraatide hulka kuuluvad Na2CO3 · H2O, Na2CO3 · 7H2O ja Na2CO3 · 10h2o. Naatriumkarbonaat lahustub kergesti vees ja glütseroolis. 20 kraadi juures võib igas 100 g vees lahustuda 20 g naatriumkarbonaati ja maksimaalne lahustuvus on 35,4 kraadi. 100 g vees võib lahustada 49,7 g naatriumkarbonaati, mis lahustub vähesel määral absoluutses etanoolis, kuid lahustub halvasti propanoolis.
Tema keemilised omadused on järgmised:
Naatriumkarbonaadi vesilahus on leeliseline ja teatud määral söövitav. See võib reageerida happe ja mõnede kaltsiumi- ja baariumisooladega. Lahus on aluseline ja võib muuta fenoolftaleiini punaseks.
(1) Stabiilsus – tugev stabiilsus, kuid see võib ka kõrgel temperatuuril laguneda, moodustades naatriumoksiidi ja süsinikdioksiidi:
![]()
Pikaajaline kokkupuude õhuga võib absorbeerida õhus olevat niiskust ja süsinikdioksiidi, tekitada naatriumvesinikkarbonaati ja moodustada kõvasid plokke:
![]()
Naatriumkarbonaadi kristalne hüdraat (Na2CO3 · 10h2o) on kuivas õhus kergesti ilmastikukindel:
![]()
(2) Termodünaamiline funktsioon – termodünaamiline funktsioon (298,15K, 100k):
Olek: tahkis
Standardne molaarse moodustumise entalpia: -1130,8 kJ · mol-1
Standardne molaarne Gibbsi moodustumise vaba energia: -1048,1 kJ · mol-1
Standardne entroopia: 138,8 J · mol-1 · K-1
(3) Hüdrolüüsireaktsioon – kuna naatriumkarbonaat hüdrolüüsitakse vesilahuses, ühendatakse ioniseeritud karbonaadiioonid vees vesinikioonidega, moodustades vesinikkarbonaadi ioonid, mille tulemuseks on vesinikioonide redutseerimine lahuses ja ülejäänud ioniseeritud hüdroksiidioonid, nii et Lahuse pH on aluseline.
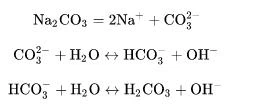
Kuna karbonaat võib ühineda prootonitega (st vesinikioonidega) vees, moodustades vesinikkarbonaati ja süsihapet, ning võib ühineda prootonitega happes, vabastades süsinikdioksiidi. Seetõttu kuulub naatriumkarbonaat happe-aluse prootoniteoorias Bronstedi alusele.
(4) Reaktsioon happega – Võtke näiteks vesinikkloriidhape. Kui vesinikkloriidhappest piisab, tekivad naatriumkloriid ja süsihape ning ebastabiilne süsihape laguneb kohe süsihappegaasiks ja veeks. Seda reaktsiooni saab kasutada süsinikdioksiidi valmistamiseks:
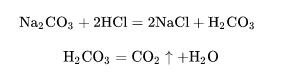
Üldine keemiline võrrand on järgmine:
![]()
Kui vesinikkloriidhape on väike, tekivad järgmised reaktsioonid:
![]()
Naatriumkarbonaat võib reageerida sarnaselt teist tüüpi hapetega.
(5) Reaktsioon leelis-naatriumkarbonaadiga võib läbida kahekordse lagunemisreaktsiooni leelisega, nagu kaltsiumhüdroksiid ja baariumhüdroksiid, et tekitada sadet ja naatriumhüdroksiid. Seda reaktsiooni kasutatakse tavaliselt tööstuses seebikivi valmistamiseks (üldtuntud kui kaustiseerimine):
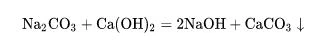
(6) Reaktsioon soolaga
Naatriumkarbonaat võib läbida kahekordse lagunemisreaktsiooni kaltsiumisoola ja baariumisoolaga, moodustades sademe ja uue naatriumsoola:

Kuna naatriumkarbonaat hüdrolüüsitakse vees, et tekitada naatriumhüdroksiid ja süsihape, sunnib selle reaktsioon mõnede sooladega keemilise tasakaalu positiivses suunas liikuma, et tekitada vastav leelis ja süsinikdioksiid:

Kokkuvõtteks võib öelda, et sellel on palju keemilisi omadusi, mis määrab ka selle laia kasutusala. Naatriumkarbonaat on üks olulisi keemilisi tooraineid. Seda kasutatakse laialdaselt kergetööstuses, igapäevases keemiatööstuses, ehitusmaterjalide, keemiatööstuses, toiduainetööstuses, metallurgia-, tekstiili-, nafta-, riigikaitse-, meditsiini- ja muudes valdkondades. Seda kasutatakse ka toorainena, puhastusvahendina ja pesuainena muude kemikaalide valmistamisel, samuti fotograafias ja analüüsides. Järgnesid metallurgia-, tekstiili-, nafta-, riigikaitse-, meditsiini- ja muud tööstused. Klaasitööstus on suurim sooda tarbija, kus ühe tonni klaasi kohta kulub 0,2 T soodat. Seda kasutatakse peamiselt floatklaasi, kineskoopklaasi kesta, optilise klaasi jms jaoks. Tööstuslikust soodast moodustavad umbes 2/3 kergetööstuse, ehitusmaterjalide ja keemiatööstuse, millele järgnevad metallurgia, tekstiil, nafta, riigikaitse, meditsiin ja muudes tööstusharudes. Kasutatakse keemiatööstuses, metallurgias jne. Raske sooda kasutamine võib vähendada leelisetolmu lendumist, vähendada tooraine tarbimist, parandada töötingimusi, parandada toote kvaliteeti, vähendada leelise erosiooni pulber tulekindlatele materjalidele ja pikendab ahjude kasutusiga. Puhvri, neutralisaatori ja taignaparandajana saab seda kasutada kookides ja jahutoitudes ning seda saab kasutada sobivas koguses vastavalt tootmisvajadustele.
Väga palju on ka naatriumkarbonaadi väljatöötamist, viidates peamiselt looduslikust leelisest sooda valmistamise meetodi arendamisele: ① juba 1849. aastal leidsid pioneerid USA-s Wyomingi osariigis magusa vee jõest naatriumvesinikkarbonaadi ning kasutasid seda pesemisel ja farmaatsias. . 1905. aastal viidi läbi esimene sooda proovitootmine, kasutades Californias Searsi järve looduslikku soodat. 1938. aastal, kui USA kütusevarustusettevõte Intermountain uuris Wyomingi osariigis Greeni jõe vesikonnas naftat ja gaasi, avastas ta maailma suurima naatriumkarbonaadirikka loodusliku leelisemaardla. 1976. aastal moodustas Ameerika Ühendriikides loodusliku leelise abil toodetud sooda 70 protsenti kogutoodangust ja 1982. aastal 94 protsenti kogutoodangust, aastase tootmisvõimsusega 9,5 miljonit tonni. ② Alates 1960. aastatest on Nõukogude Liit töötlenud alumiiniumoksiidi nefeliiniga (naatriumi, kaaliumi, alumiiniumi ja ränioksiidi sisaldav looduslik leeliskivi) ning tootnud samaaegselt soodat, kaaliumkloriidi ja tsementi, realiseerides industrialiseerimise, nii et nefeliini toorainet saab laialdaselt kasutada ilma jäätmete ärajuhtimine. 1975. aastaks oli rajatud viis nefeliini töötlemise tehast.

